Морская вода является бесконечным источником металлов, минералов, питьевой воды, кислорода и водорода. Учёные всех стран десятилетиями ищут возможность добывать эти богатства из морских и океанских глубин. Главная задача — делать работы экономически выгодно, но именно с этим связаны все барьеры на пути разработчиков. В Китае решили одну из этих проблем — научились простой добыче водорода без лишних затрат.
Водород извлекается из воды в процессе электролиза. Это простая и понятная операция, но только если добывать этот газ из чистой воды. Добыча водорода непосредственно из морской воды требует предварительного опреснения или очень сложных установок. Растворённые в морской воде соли (ионы) металлов и минералов разрушают катализаторы электролизёров и другие узлы устройств, как и требуют работы насосов для прокачки морской воды.
Учёные из Нанкинского технического университета в Китае в журнале Nature рассказали об уникальной установке, которая лишена всех указанных выше недостатков. Без насосов и быстрого износа катализаторов она способна длительное время добывать водород и кислород прямо из морской воды.
«Наша стратегия реализует эффективный, гибкий по размеру и масштабируемый прямой электролиз морской воды, аналогичный расщеплению пресной воды, без заметного увеличения эксплуатационных расходов», — сказал Цзунпин Шао (Zongping Shao), профессор химической инженерии из Нанкинского технического университета в Китае.
Для защиты катализаторов от воздействия морской воды — солей и ионов — предложено интересное решение. Покрытые катализатором электроды, на которых вырабатывается водород и кислород (один на катоде, а другой на аноде), никогда не контактируют с морской водой. От этого их защищает насыщенный электролит в виде гидроксида калия, в который эти электроды погружены. Как же туда попадает вода?
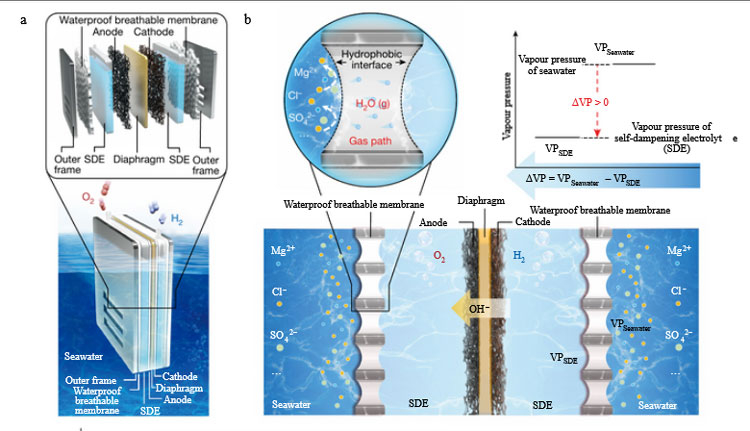
Электролит с обеих сторон электродов защищён мембраной. Богатая фтором мембрана пропускает водяной пар, но не жидкость. Через мембрану в электролит попадает только водяной пар, оставляя соли в морской воде. В электролите пар снова превращается в воду и расщепляется на водород и кислород как опреснённая вода без негативных последствий для катализаторов. Подкачка пара в электролит идёт за счёт внешнего избыточного давления и не требует насосов.
Насосы нужны разве что для прокачки морской воды, но в случае электролиза с пресной водой они тоже будут нужны, так что это не увеличивает накладные расходы. Более того, из воды с повышенной концентрацией солей удобно и выгодно добывать минералы и металлы, например, тот же литий или уран.
Исследователи на практике доказали работу инновационной установки. Демонстратор из 11 электролизных ячеек опустили в воды залива Шэньчжэнь, где он проработал без остановки 130 дней. Каждый час установка вырабатывала 386 л водорода. Затраты электричества шли только на подкачку свежей морской воды и на сам процесс электролиза. Система отлично себя показала в испытаниях, хотя о коммерческом внедрении говорить пока рано. Учёные планируют значительно повысить её эффективность, для чего необходимы эксперименты с разными составами электролита и катализаторов.